Imunoterapia a devenit o reală speranță pentru pacientele cu cancer de col uterin avansat, acolo unde tratamentele clasice, precum chimioterapia sau radioterapia, au adus beneficii limitate în formele recurente sau metastatice. În acest articol, îți prezentăm mecanismele prin care sistemul imunitar poate recunoaște și combate mai eficient celulele tumorale cervicale, mai ales la pacientele infectate cu tulpini oncogene HPV. Vei afla care sunt cele mai importante rezultate ale unor studii clinice privind imunoterapia în tratamentul cancerului de col uterin și ce beneficii oferă această terapie pacientelor.

Cercetările recente arată că imunoterapia poate crește șansele de răspuns la tratament în cancerul de col uterin
Imunoterapia în cancer col uterin avansat. Mecanisme moleculare și fundament biologic
Cancerul de col uterin avansat, fie că este persistent, recurent sau metastazat, reprezintă una dintre cele mai dificile provocări din practica ginecologică și oncologică modernă. Deși screeningul citologic și, mai recent, testarea HPV, alături de programele de vaccinare anti-HPV, au contribuit semnificativ la scăderea incidenței formelor incipiente de boală, un număr considerabil de paciente continuă să se confrunte cu forme avansate și agresive ale acestei patologii. În aceste cazuri, opțiunile terapeutice convenționale – precum chimioterapia, terapia antiangiogenică sau radioterapia – oferă beneficii limitate, iar prognosticul rămâne rezervat.
Cancerul de col uterin este strâns asociat cu infecția persistentă cu virusul papilloma uman (HPV), în special tulpinile oncogene 16 și 18. Aceste tulpini virale determină transformări maligne la nivelul celulelor epiteliale cervicale, în principal prin expresia proteinelor E6 și E7. Aceste proteine virale interferează cu mecanisme esențiale de control al ciclului celular și al apoptozei, cum ar fi p53 și Rb, inducând instabilitate genomică și favorizând acumularea de mutații care pot duce la dezvoltarea cancerului.
În acest context, sistemul imun joacă un rol esențial în recunoașterea și eliminarea celulelor transformate. Totuși, tumorile cervicale dezvoltă adesea mecanisme sofisticate de evaziune imună. Microambientul tumoral devine imunotolerant, caracterizat prin infiltrarea cu celule T reglatorii, macrofage cu fenotip protumoral (M2), și, mai ales, prin expresia crescută a moleculelor imunoinhibitoare precum PD-L1 (programmed death-ligand 1).
PD-1 (programmed cell death protein 1) este un receptor aflat pe suprafața limfocitelor T, iar interacțiunea sa cu PD-L1 exprimat de celulele tumorale sau de alte celule din microambientul tumoral induce o stare de epuizare funcțională a limfocitelor T. Acest fenomen inhibă eficiența răspunsului imun antitumoral, permițând tumorii să se dezvolte și să se răspândească necontrolat.
Imunoterapia cu inhibitori ai punctelor de control imun, în special cei care țintesc axa PD-1/PD-L1, a revoluționat tratamentul multor tipuri de cancer, inclusiv cancerul de col uterin avansat. Aceste terapii – reprezentate de medicamente precum pembrolizumab și nivolumab - blochează interacțiunea dintre PD-1 și PD-L1, restabilind astfel activitatea citotoxică a limfocitelor T și facilitând distrugerea celulelor tumorale.
Un avantaj important al cancerului de col uterin din perspectiva imunoterapiei este determinarea sa virală. Prezența infecției HPV determină generarea unui număr crescut de neoantigene virale, care pot stimula mai ușor un răspuns imun. De asemenea, instabilitatea genomică asociată cu transformarea malignă contribuie la crearea unui profil antigenic divers, favorabil activării răspunsului imun sub influența terapiei. Astfel, blocada punctelor de control imun oferă o strategie terapeutică inovatoare și promițătoare pentru pacientele cu forme avansate, refractare sau recidivante de cancer cervical. Această abordare reechilibrează răspunsul imun antitumoral și, în multe cazuri, poate duce la remisiuni durabile sau la control pe termen lung al bolii – acolo unde terapiile clasice eșuează.
Pe de altă parte, imunoterapia nu este o soluție universală; eficacitatea ei depinde de o serie de factori: existența antigenelor țintă, nivelul infiltrării imunelor, prezența biomarkerilor predictivi (de ex. expresia PD-L1, TMB, statutul RMM/instabilitate microsatelitară) și rezistența intrinsecă sau dobândită a tumorii. De aceea, rolul imunoterapiei în cancerul de col nu este doar de a adăuga o armă nouă, ci de a integra un tratament personalizat, bazat pe selecția pacientelor potrivite.
Progrese și studii clinice în imunoterapia cancerului de col uterin avansat
Un moment definitoriu pentru validarea imunoterapiei în cancerul de col uterin a fost studiul de fază III KEYNOTE-826, un studiu randomizat care a evaluat adăugarea pembrolizumab la chimioterapia standard (cu sau fără bevacizumab) în tratamentul de primă linie al pacientelor cu cancer cervical persistent, recurent sau metastatic.
Rezultatele finale au demonstrat un beneficiu semnificativ în ceea ce privește supraviețuirea globală (OS) și supraviețuirea fără progresie (PFS) în rândul pacientelor care au primit pembrolizumab, comparativ cu chimioterapia standard. Acest beneficiu a fost clar evidențiat în subgrupul cu CPS (Combined Positive Score) ≥ 1, dar și în populația generală, indiferent de expresia PD-L1. Riscul de deces a fost redus cu aproximativ 40% în rândul pacientelor cu CPS ≥ 1. De asemenea, toxicitățile severe asociate au fost considerate gestionabile, fără a compromite în mod semnificativ calitatea vieții pacientelor, conform analizei parametrilor PRO (patient-reported outcomes).
Subanalizele pe subgrupuri din KEYNOTE-826 au arătat că beneficiul în supraviețuire s-a menținut indiferent de:
-
utilizarea sau nu a bevacizumabului,
-
alegerea agentului platinat (cisplatin vs. carboplatin),
-
histologia tumorală (scuamoasă sau non-scuamoasă),
-
antecedentele de radioterapie cu chimioterapie.
Un alt studiu, retrospectiv, recent, care a evaluat 56 de paciente cu cancer cervical metastatic, a raportat că pacientele care au primit imunoterapie (ca monoterapie sau în combinație cu bevacizumab) au prezentat o rată de răspuns obiectiv (ORR) de 94%, comparativ cu 32% în grupul care nu a primit imunoterapie. De asemenea, supraviețuirea fără progresie la 12 luni a fost semnificativ mai mare în grupul tratat cu imunoterapie: 94,4% vs. 59,7%. Deși este un studiu cu un eșantion redus și limitări metodologice, rezultatele sale susțin concluziile din KEYNOTE-826, sugerând un beneficiu clinic important al imunoterapiei în practica reală.
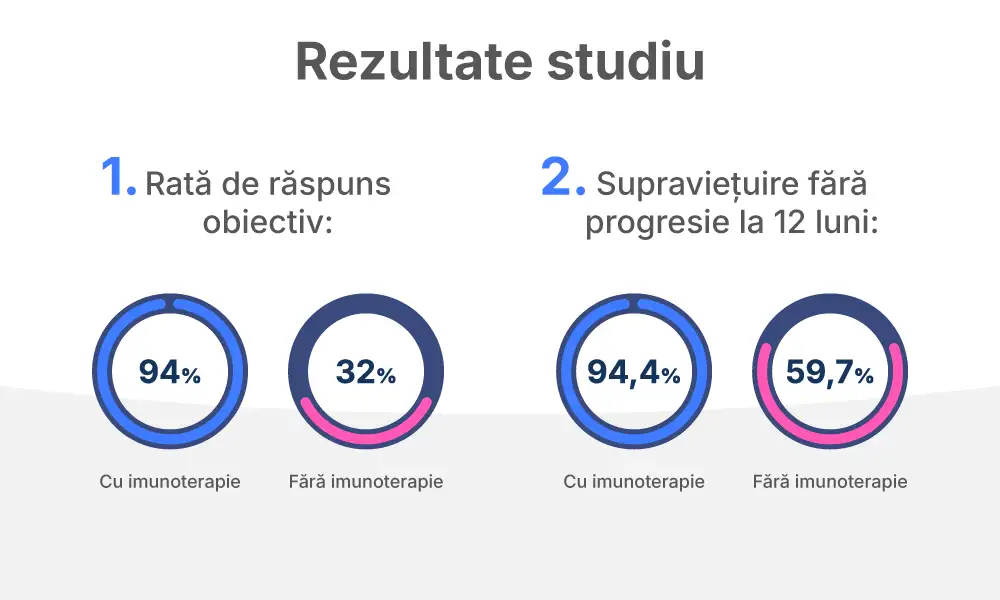
Rezultatele studiului sugerează un beneficiu clinic important al imunoterapiei
Alte direcții și terapii investigate – studii cu Nivolumab și combinații ICI
Un alt agent imunoterapic important, nivolumab, a fost investigat în mai multe studii. Studiul de fază II NRG-GY002 a evaluat monoterapia cu nivolumab la paciente cu cancer cervical persistent sau recurent, anterior tratate cu chimioterapie pe bază de platină. Rezultatele au arătat o activitate clinică modestă: doar una dintre cele 25 de paciente a avut răspuns parțial (4%), iar 9 au prezentat boală stabilă, cu o durată medie a stabilizării de 5,7 luni. Deși tratamentul a fost în general bine tolerat, aceste date indică faptul că monoterapia cu nivolumab este insuficientă în majoritatea cazurilor, justificând explorarea combinațiilor cu alte terapii.
În acest sens, studiul CheckMate 358, de fază I/II, a evaluat nivolumab în monoterapie sau în asociere cu ipilimumab. Pentru pacientele cu cancer cervical recurent sau metastatic, rata de răspuns obiectiv (ORR) la nivolumab a fost de aproximativ 26,3%, cu o durată promițătoare a răspunsului și o supraviețuire globală mediană de 21,9 luni. Mai important, combinația nivolumab + ipilimumab a crescut rata de răspuns la aproximativ 40%, sugerând că asocierea inhibitorilor de checkpoint (ICI) ar putea depăși limitările terapiei imunologice în monoterapie.

Studiul arată că imunoterapia cu Nivolumab, în monoterapie sau asociat cu ipilimumab, oferă rezultate promițătoare în cancerul cervical recurent sau metastatic
Un alt studiu relevant este NiCOL, care a investigat utilizarea nivolumab concomitent cu chemoradioterapie și brahiterapie, urmată de tratament de întreținere, la pacientele cu boală local avansată. Studiul a arătat că această abordare este fezabilă, cu profil de siguranță acceptabil, iar rezultatele inițiale sunt promițătoare. Acest tip de terapie integrativă oferă o direcție nouă pentru includerea imunoterapiei chiar și în formele local avansate, nu doar în cele metastatice sau recidivante.
Alte rezultate importante: Studiul BEATcc
O evoluție interesantă și în același timp controversată a fost publicată în 2025, în urma studiului BEATcc, care a evaluat adăugarea atezolizumab (un inhibitor PD-L1) la chimioterapie + bevacizumab. Rezultatele au arătat un beneficiu clinic semnificativ, dar, surprinzător, independent de expresia PD-L1. Această constatare pune sub semnul întrebării rolul PD-L1 ca biomarker predictiv robust pentru selecția pacientelor care pot beneficia de imunoterapie. Dacă aceste rezultate vor fi confirmate de analize suplimentare, ele pot simplifica decizia terapeutică, eliminând necesitatea testării expresiei PD-L1 înainte de inițierea tratamentului.
Perspective viitoare: vaccinuri terapeutice și terapii celulare
Pe lângă inhibitorii de puncte de control imun deja disponibili, cercetarea în domeniu explorează noi direcții promițătoare, precum vaccinurile terapeutice HPV și terapiile celulare adoptive.
Printre strategiile emergente se numără:
-
vaccinurile terapeutice direcționate împotriva antigenelor virale E6 și E7 ale HPV;
-
utilizarea limfocitelor T infiltrante tumoral (TILs);
-
ingineria receptorilor T (TCR) specifici pentru antigenele HPV.
Aceste abordări au potențialul de a genera răspunsuri imunologice mai specifice și mai durabile, însă sunt în mare parte în faze experimentale, iar implementarea lor este limitată de provocări tehnice, costuri ridicate și logistică complexă.
Selecția pacientelor pentru imunoterapie în cancer col uterin: importanța biomarkerilor și evaluarea clinică individualizată
În era oncologiei de precizie, unul dintre cele mai importante aspecte ale practicii medicale moderne este selecția riguroasă a pacientelor care pot beneficia cu adevărat de tratamente imunoterapice. Această etapă este esențială, întrucât eficiența imunoterapiei depinde nu doar de profilul biologic al tumorii, ci și de caracteristicile individuale ale pacientei. Cu alte cuvinte, nu toate pacientele cu cancer de col uterin avansat sunt candidate ideale pentru imunoterapie, iar decizia trebuie fundamentată atât pe date moleculare, cât și pe evaluarea clinică detaliată.
În prezent, cel mai utilizat biomarker pentru orientarea tratamentului imunologic în cancerul de col uterin este expresia proteinei PD-L1 (programmed death-ligand 1) în țesutul tumoral. Această expresie este evaluată printr-o metodă numită imunohistochimie, care permite vizualizarea proteinelor direct în probele de țesut tumoral recoltate prin biopsie. Expresia PD-L1 este interpretată cu ajutorul unui scor numit Combined Positive Score (CPS), care ține cont de proporția de celule tumorale și celule ale sistemului imunitar (precum limfocitele sau macrofagele) care exprimă PD-L1, raportat la numărul total de celule din eșantionul analizat. În majoritatea studiilor clinice, un CPS mai mare sau egal cu 1 este considerat un prag minim pentru a anticipa o probabilitate crescută de răspuns favorabil la terapia cu inhibitori PD-1, cum este pembrolizumab.
Cu toate acestea, expresia PD-L1 nu este un marker perfect. Există situații în care paciente cu scoruri PD-L1 scăzute răspund bine la tratament, dar și cazuri în care expresia este ridicată, iar răspunsul lipsește sau este modest. Această lipsă de concordanță între biomarker și eficacitatea clinică a tratamentului a condus la intensificarea cercetărilor pentru identificarea unor markeri suplimentari, mai preciși, care să permită o selecție mai bună a pacientelor eligibile.
Printre acești biomarkeri emergenți se numără încărcătura mutațională tumorală (TMB – tumor mutational burden), care reflectă numărul total de mutații genetice prezente în ADN-ul celulei canceroase. Un TMB ridicat sugerează că tumora produce mai multe proteine anormale, care pot fi recunoscute mai ușor de sistemul imun, crescând astfel șansa de răspuns la imunoterapie. De asemenea, un alt domeniu investigat intens este reprezentat de mutațiile genelor implicate în mecanismele de reparare a ADN-ului. Atunci când aceste mecanisme sunt afectate, celulele tumorale acumulează mutații într-un ritm mai accelerat, generând un profil imunogen crescut, cu potențial de răspuns la terapiile imunologice.
Instabilitatea microsatelitară (MSI) și defectele de reparare a erorilor de replicare a ADN-ului (cunoscute sub denumirea de dMMR – mismatch repair deficiency) sunt alte două trăsături moleculare care au fost asociate cu un răspuns foarte bun la inhibitori PD-1, în special în cancerele colorectale, endometriale sau gastrice. În cancerul de col uterin, aceste caracteristici sunt însă rar întâlnite, iar rolul lor ca biomarkeri predictivi este considerat limitat, dar nu complet neglijabil.
Un alt domeniu de interes este evaluarea infiltratului limfocitar tumoral (TILs – tumor infiltrating lymphocytes), care reflectă prezența celulelor imune direct în microambientul tumoral. Un număr crescut de limfocite T active în interiorul tumorii poate sugera o încercare a sistemului imun de a recunoaște și elimina celulele canceroase, ceea ce poate fi amplificat prin blocada punctelor de control imun, cum este cea realizată de imunoterapia cu inhibitori PD-1/PD-L1. În plus, se investighează și profilul acestor limfocite – dacă sunt celule T citotoxice, celule T reglatorii sau alte tipuri – precum și expresia anumitor markeri de activare sau imunosupresie care pot influența răspunsul la tratament.
Deși, în prezent, nu sunt utilizate de rutină în practica clinică, unele abordări experimentale vizează și evaluarea expresiei antigenelor virale E6 și E7 ale HPV, proteine virale implicate direct în transformarea malignă a celulelor cervicale. Această evaluare ar putea deveni relevantă în viitor pentru strategiile de imunoterapie avansată, cum ar fi vaccinurile terapeutice personalizate sau terapiile celulare adoptive.
Imunoterapie cancer: cine poate urma tratamentul?
Pe lângă profilul molecular, selecția candidatelor pentru imunoterapie trebuie să țină cont în mod esențial și de evaluarea clinică individuală. Starea generală a pacientei, evaluată prin scoruri precum ECOG (Eastern Cooperative Oncology Group), este un factor-cheie în luarea deciziei, deoarece tratamentele imunologice pot avea reacții adverse semnificative, mai ales la pacientele fragile sau cu afecțiuni cronice. Prezența comorbidităților, cum ar fi boli autoimune active, afecțiuni hepatice sau pulmonare severe, poate contraindica imunoterapia, sau cel puțin poate necesita o monitorizare atentă.
La fel de importante sunt istoricul oncologic al pacientei, tratamentele anterioare (chirurgicale, chimioterapice sau radioterapice), precum și gradul de diseminare al bolii. De exemplu, pacientele cu metastaze multiple și afectare viscerală extinsă pot avea un răspuns mai slab, în timp ce cele cu boală mai limitată și status imun bun pot beneficia mai mult de tratamente imunologice.
În mod ideal, decizia de inițiere a imunoterapiei trebuie luată în cadrul unui consiliu oncologic multidisciplinar, care să includă oncologul medical, ginecologul oncolog, anatomopatologul, radiologul și dacă este posibil, un imunolog sau un specialist în genetică moleculară. Această abordare colaborativă permite interpretarea corectă a datelor moleculare, evaluarea realistă a stării pacientei și stabilirea unui plan terapeutic personaliz
at, în care beneficiile imunoterapiei sunt maximizate, iar riscurile sunt atent controlate.
Este important de reținut că nu toate pacientele cu cancer de col uterin avansat sunt potrivite pentru imunoterapie, iar o selecție atentă reduce riscul inițierii unui tratament ineficient sau chiar periculos. Tocmai de aceea, pe măsură ce datele științifice se acumulează, se dezvoltă tot mai multe instrumente de selecție a pacientelor, care combină datele moleculare cu algoritmi clinici, pentru a crește șansele de succes și a oferi o îngrijire personalizată, sigură și eficientă.
Accesul la imunoterapie în cancerul de col uterin în România și Uniunea Europeană (2026)
În ultimii ani, imunoterapia a devenit un standard terapeutic pentru multiple tipuri de cancer, inclusiv în formele avansate de cancer de col uterin, datorită rezultatelor promițătoare demonstrate în studii clinice internaționale precum KEYNOTE-826 și CheckMate 358. În Uniunea Europeană, inclusiv în România, accesul la aceste terapii inovatoare este reglementat de mai multe instituții – în primul rând Agenția Europeană a Medicamentului (EMA), dar și autoritățile naționale precum Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România (ANMDMR) și Casa Națională de Asigurări de Sănătate (CNAS).
Aprobări EMA și poziționarea imunoterapiei în ghidurile europene
În anul 2021, EMA a aprobat pembrolizumab pentru utilizare în combinație cu chimioterapia, cu sau fără bevacizumab, ca tratament de primă linie în cancerul de col uterin recurent sau metastatic la pacientele cu expresie PD-L1 CPS ≥ 1. Această decizie a fost luată pe baza datelor solide din studiul KEYNOTE-826, care a demonstrat o reducere semnificativă a riscului de deces și o prelungire semnificativă a supraviețuirii fără progresie. Ghidurile ESMO (European Society for Medical Oncology) din 2023–2024 au inclus această combinație ca opțiune de tratament de primă intenție la pacientele eligibile, recomandând testarea expresiei PD-L1 ca parte a algoritmului standard de evaluare la diagnostic.
În paralel, alte imunoterapii, precum nivolumab și atezolizumab, se află în diferite faze de evaluare sau aprobare, unele în regim de utilizare compasională sau în cadrul studiilor clinice, altele fiind deja aprobate pentru alte tipuri de cancer, dar investigate activ în cancerul cervical.
Disponibilitatea tratamentelor în România (2026)
În România, imunoterapia a devenit treptat accesibilă pacientelor cu cancer de col uterin începând cu anii 2022–2023, în urma includerii pembrolizumabului în lista medicamentelor compensate și gratuite pentru indicația aprobată de EMA. Până în 2025, tratamentul era deja disponibil în centrele mari oncologice din rețeaua publică (Institutul Oncologic București, Cluj, Iași, Timișoara etc.) și în unele rețele private acreditate, în condiții de rambursare totală sau parțială, în funcție de protocolul individualizat.
Cu toate acestea, accesul rămâne inegal la nivel național, în special în spitalele județene sau în zonele rurale, unde lipsa echipelor multidisciplinare, a echipamentelor pentru testarea biomarkerilor (PD-L1, TMB, MSI) și a personalului specializat limitează aplicarea tratamentelor moderne. De asemenea, unele paciente se confruntă cu întârzieri administrative legate de aprobarea dosarelor de tratament de către comisiile de specialitate sau de disponibilitatea efectivă a medicamentelor la farmaciile cu circuit închis ale spitalelor.
Pentru a beneficia de imunoterapie, pacientele trebuie, de regulă, să îndeplinească o serie de criterii clinice și biologice clare:
-
diagnostic confirmat de cancer de col uterin recurent sau metastatic;
-
test imunohistochimic pozitiv pentru PD-L1 cu scor CPS ≥1 (în cazul pembrolizumabului);
-
stare generală bună (ECOG 0-1);
-
lipsa contraindicațiilor severe, cum ar fi boli autoimune active, infecții cronice necontrolate sau afectări organice majore.
După depunerea documentației la comisia oncologică județeană sau națională, aprobarea tratamentului durează în medie 5–10 zile lucrătoare. Totuși, unele paciente relatează întârzieri mai mari din cauza birocrației sau a lipsei de personal în instituțiile care gestionează aceste dosare.
Acces prin studii clinice și programe compasionale
Pentru pacientele care nu se califică pentru imunoterapie prin programele standard (de exemplu, în caz de PD-L1 negativ sau în linii terapeutice ulterioare), există opțiunea includerii în studii clinice, disponibile în marile centre universitare sau în spitalele private acreditate. România participă la mai multe studii internaționale care investighează noi combinații de imunoterapie, terapii celulare, vaccinuri HPV terapeutice și noi biomarkeri predictivi.
De asemenea, în anumite situații, medicamentele imunoterapice pot fi oferite prin programe compasionale sau prin fonduri speciale, în funcție de gravitatea cazului și de disponibilitatea medicamentelor din partea producătorilor. Este important ca pacientele să fie informate corect cu privire la aceste opțiuni, deoarece accesul depinde și de inițiativa medicului curant și de colaborarea cu sponsorii studiilor sau cu firmele farmaceutice.
Protocol de tratament și strategie terapeutică în România
În contextul actual, pentru paciente cu cancer cervical persistent, recurent sau metastatic care sunt considerate eligibile (de exemplu, cu PD-L1 CPS ≥ 1 sau în studii clinice), se poate propune schema care include pembrolizumab în asociere cu chimioterapia standard (paclitaxel + cisplatin sau carboplatin), cu sau fără bevacizumab, conform datelor din studiul KEYNOTE-826. Această combinație a demonstrat un beneficiu de supraviețuire semnificativ și este deja considerată un potențial standard de tratament în numeroase ghiduri internaționale. În România, implementarea acestei strategii trebuie realizată cu atenție la accesul medicamentelor, aprobările naționale și posibilul suport din rețele oncologice.
Tratamentul se administrează de regulă în cicluri (de exemplu la fiecare 3 săptămâni) până la maximum 35 de cicluri de pembrolizumab (aproximativ 2 ani) sau până la progresie sau apariția toxicităților inacceptabile. Durata de 2 ani a fost frecvent utilizată în studiile clinice. Monitorizarea periodică include imagistică (scanări CT sau RMN conform protocoalelor oncologice), analize de sânge uzuale, evaluarea funcției hepatice, renale, tiroidiene, precum și solicitarea oricăror simptome sugestive de reacții imune (diaree, tuse, dispnee, dureri abdominale, febră etc.).
În situația în care boala progresează sau apare rezistență, opțiunile pot include imunoterapie în monoterapie sau în combinații experimentale (de exemplu, cu alte ICI, agenți țintiți, antiangiogenici) sau includerea pacientei în studii clinice locale sau internaționale. În plus, pentru cazurile locale avansate nerezecabile, în unele studii se investighează adăugarea imunoterapiei concomitent cu radioterapia și chimioterapia pentru a crea un efect sinergic și a sensibiliza tumorile la tratamentul locoregional. Este important ca centrele oncologice din marile spitale din România să colaboreze la implementarea studiilor clinice de imunoterapie și să faciliteze accesul pacientelor eligibile, prin rețele de referință, comitete tumorale și suport logistic.
Inhibitorii PD-1/PD-L1 aprobați și terapiile inovatoare în 2026
În momentul actual, inhibitorii PD-1 reprezintă standardul de aur al imunoterapiei pentru cancerul de col uterin avansat.
Pembrolizumab este primul și cel mai bine studiat medicament anti-PD-1 aprobat atât de Agenția Europeană a Medicamentului (EMA), cât și de FDA. Pembrolizumab poate fi utilizat în monoterapie în linia a doua, după eșecul chimioterapiei, sau în combinație cu chimioterapia standard (carboplatină și paclitaxel) și bevacizumab în prima linie, pentru paciente cu tumori PD-L1 pozitive. Schema de administrare este standardizată: infuzie intravenoasă o dată la trei săptămâni, cu continuarea tratamentului până la progresia bolii sau toxicități inacceptabile.
Nivolumab este o altă opțiune anti-PD-1, aflată în prezent în studiile clinice și utilizată pe scară restrânsă în anumite centre, cu rezultate promițătoare. De asemenea, alte imunoterapice precum dostarlimab și atezolizumab (anti-PD-L1) sunt în curs de aprobare sau studiu clinic pentru această indicație, cu potențial de a extinde arsenalul terapeutic.
Mai mult, este studiată combinarea inhibitorilor PD-1/PD-L1 cu inhibitori CTLA-4 (cum ar fi ipilimumab), care au un mecanism complementar de activare a sistemului imunitar, pentru a crește rata de răspuns și durata acestuia. Aceste combinații sunt încă în studii clinice și pot deschide noi perspective terapeutice în următorii ani.
Alte direcții în cercetare includ utilizarea terapiei cu celule T adoptive, vaccinurile terapeutice împotriva antigenelor HPV și utilizarea medicamentelor epigenetice care pot modifica expresia genică tumorală pentru a crește imunodetectabilitatea. Toate aceste strategii ar putea, în viitorul apropiat, să extindă considerabil opțiunile terapeutice disponibile.
Profilul de siguranță al imunoterapiei în cancerul de col uterin: ce trebuie să știe pacientele
Deși imunoterapia revoluționează tratamentul cancerului de col uterin avansat, aducând beneficii importante în ceea ce privește prelungirea supraviețuirii și menținerea unei calități a vieții acceptabile, această clasă terapeutică nu este lipsită de riscuri. Medicamentele din categoria inhibitorilor punctelor de control imun, cum sunt pembrolizumab sau nivolumab, acționează prin „deblocarea” sistemului imunitar, astfel încât celulele T ale organismului să poată recunoaște și distruge celulele tumorale. Odată ce sistemul imun este stimulat în mod susținut, există riscul ca acesta să reacționeze și împotriva țesuturilor normale, ceea ce poate duce la apariția unor reacții adverse autoimune.
Aceste efecte secundare sunt denumite reacții adverse imun-mediate și pot afecta orice organ sau sistem, de la piele, tiroidă și intestin, până la plămâni, ficat sau rinichi. Cele mai frecvente efecte secundare raportate în studiile clinice, precum KEYNOTE-826 sau CheckMate 358, sunt erupțiile cutanate, pruritul (mâncărimea), diareea, oboseala persistentă și modificările tiroidiene (hipotiroidism sau, mai rar, hipertiroidism). Aceste reacții sunt, de regulă, de grad ușor sau moderat (grad 1-2) și pot fi gestionate eficient cu tratament simptomatic sau, în unele cazuri, cu corticosteroizi în doze mici.
Reacțiile de grad 3 sau 4, care sunt considerate severe și pot pune viața în pericol, sunt mai rare, dar necesită intervenție medicală rapidă. Acestea pot include pneumonita (inflamația plămânilor), hepatita autoimună (cu creșteri importante ale transaminazelor), colita (inflamația colonului cu diaree severă), nefrita (inflamația rinichilor), miocardita (inflamația mușchiului cardiac) sau afectări neurologice (precum polinevrite sau encefalite). De aceea, este esențial ca pacientele aflate în tratament cu imunoterapie să fie monitorizate atent, prin consulturi regulate și analize de sânge periodice, în special pentru funcția hepatică, renală, tiroidiană și pulmonară.
Un alt aspect important este faptul că aceste reacții adverse pot apărea în orice moment al tratamentului, dar și la săptămâni sau luni după încheierea terapiei, motiv pentru care urmărirea trebuie continuată chiar și după oprirea administrării medicamentului. În general, reacțiile autoimune răspund bine la întreruperea temporară a imunoterapiei și la administrarea de medicamente imunosupresoare, în special cortizonice. În cazuri mai rare, este necesară intervenția medicilor de alte specialități – gastroenterologi, endocrinologi, pneumologi sau neurologi – pentru a gestiona complicațiile specifice.
Datele din studiile clinice sugerează că, în ciuda acestor riscuri, majoritatea pacientelor tolerează imunoterapia bine, iar beneficiile în ceea ce privește controlul bolii și supraviețuirea depășesc riscurile, în special dacă pacientele sunt atent selectate și monitorizate. De exemplu, în studiul KEYNOTE-826, incidența efectelor secundare severe a fost semnificativă, dar majoritatea au fost reversibile cu tratament adecvat și nu au dus la oprirea completă a terapiei în toate cazurile. În plus, un alt avantaj important este faptul că, în comparație cu chimioterapia convențională, imunoterapia nu produce alopecie (căderea părului), nu induce greață severă și nu afectează, în mod direct, măduva osoasă, motiv pentru care multe paciente raportează o calitate a vieții superioară în timpul tratamentului.
Cu toate acestea, este extrem de important ca pacientele să fie bine informate încă de la început cu privire la semnele precoce ale reacțiilor adverse imun-mediate, astfel încât să se poată adresa rapid echipei medicale. Simptome aparent banale, precum o tuse seacă persistentă, scaune moi repetate, oboseală accentuată sau o erupție cutanată, nu trebuie ignorate, mai ales în contextul imunoterapiei.
În concluzie, deși imunoterapia are un profil de siguranță favorabil în general, ea necesită monitorizare atentă, educarea pacientei și o echipă medicală experimentată în recunoașterea și tratarea reacțiilor adverse autoimune. Colaborarea între pacientă și medic este esențială pentru a identifica rapid orice problemă și pentru a ajusta tratamentul în mod corespunzător. Astfel, șansele de succes ale imunoterapiei cresc, iar riscurile pot fi reduse semnificativ, contribuind la o experiență terapeutică sigură și eficientă.
Perspective viitoare în imunoterapia cancerului de col uterin: ce ne așteptăm în 2026?
Privind spre viitorul apropiat, imunoterapia în cancerul de col uterin se află într-un proces accelerat de evoluție, cu numeroase direcții de cercetare aflate în desfășurare. Se prefigurează transformări importante nu doar în ceea ce privește indicațiile terapeutice, ci și în modul de selecție al pacientelor, tipurile de combinații terapeutice și strategia generală de tratament.
Unul dintre cele mai promițătoare domenii de extindere a imunoterapiei este combinarea acesteia cu radioterapia în boala local avansată, unde imunoterapia ar putea juca un rol de radiosensibilizator imun. Mai multe studii de fază III aflate în desfășurare explorează această asociere. Dacă rezultatele vor demonstra siguranță și beneficii clinice este foarte posibil ca imunoterapia să fie integrată nu doar în stadiile metastatice sau recurente, ci și în formele locale agresive ale bolii, încă din fazele inițiale ale tratamentului.
În paralel, se conturează o schimbare importantă în ceea ce privește criteriile de selecție a pacientelor pentru imunoterapie. Pe măsură ce datele din studii precum BEATcc sunt analizate și publicate, este posibil ca rolul exclusiv al PD-L1 ca biomarker să se diminueze. În locul unui singur marker predictiv, selecția ar putea deveni multifactorială, bazată pe profiluri imunologice complexe, încărcătura mutațională tumorală (TMB), semnături genetice, transcriptomice sau chiar metabolomice. Această abordare ar permite o personalizare mai rafinată a tratamentului și ar putea extinde accesul la imunoterapie pentru paciente care, conform criteriilor actuale, nu sunt eligibile.
Tot în linia cercetării inovatoare, se anticipează progrese semnificative în dezvoltarea și aplicarea clinică a vaccinurilor terapeutice HPV, inclusiv pe platforme ARNm sau cu vectori virali optimizați, precum și în utilizarea terapiilor celulare adoptive. Aceasta include transferul de limfocite T infiltrante tumorale (TILs) și ingineria genetică a receptorilor de celule T (TCR) pentru recunoașterea antigenelor HPV specifice. Deși în prezent aceste terapii sunt disponibile doar în cadrul studiilor clinice, este de așteptat ca, în anii următori, ele să devină mai fezabile clinic, cu protocoale mai sigure, mai eficiente și mai ușor de implementat la scară mai largă.
Un alt trend emergent este extinderea imunoterapiei către stadii mai timpurii ale bolii, nu doar în formele avansate. Astfel, se evaluează tot mai intens rolul imunoterapiei în scop neoadjuvant (înainte de tratamentul local), concomitent (împreună cu radioterapia sau chimioterapia) sau adjuvant (după tratamentul local radical). Obiectivul este scăderea riscului de recurență și prelungirea supraviețuirii pe termen lung. Această strategie impune, însă, și adaptarea regimurilor de tratament, optimizarea duratei imunoterapiei și identificarea momentului terapeutic ideal pentru introducerea acestor agenți în algoritmul oncologic.
Pentru România, provocările rămân considerabile, însă direcțiile sunt clare. Până în 2026, unul dintre obiectivele majore ar trebui să fie dezvoltarea unei infrastructuri solide pentru cercetare și tratament imunoterapic, incluzând:
-
crearea unui registru național de paciente eligibile pentru imunoterapie;
-
extinderea accesului la testare pentru biomarkeri, precum PD-L1, TMB sau MSI, prin secvențiere genomică și evaluare imunologică avansată;
-
formarea de echipe multidisciplinare funcționale (ginecolog-oncolog, oncolog medical, patolog, imunolog), capabile să ia decizii personalizate;
-
nu în ultimul rând, implicarea activă a României în studii clinice internaționale, care să ofere acces precoce la terapii inovatoare.
Doar prin astfel de măsuri concrete, promisiunile imunoterapiei pot deveni realitate pentru cât mai multe paciente, contribuind la creșterea speranței de viață, la reducerea recurențelor și la îmbunătățirea calității vieții în cancerul de col uterin.
Întrebări frecvente și informații utile pentru paciente
Când este recomandată imunoterapia în cancerul de col uterin?
Imunoterapia cu inhibitori PD-1/PD-L1 este recomandată pentru cancerul de col uterin avansat sau metastatic, în special la recidivă sau eșec al tratamentului standard. Ghidurile actuale plasează combinația de imunoterapie și chimioterapie ca standard de primă linie pentru tumorile ce exprimă PD-L1 (CPS ≥1), decizia fiind luată multidisciplinar după evaluarea biomarkerilor.
Ce înseamnă testarea PD-L1 și cât de importantă este?
Testarea PD-L1 se efectuează pe o probă de țesut tumoral, prelevată prin biopsie, pentru a măsura expresia ligandului PD-L1. Acest ligand poate permite celulelor canceroase să se ascundă de sistemul imunitar. Rezultatul, exprimat ca Combined Positive Score (CPS), este crucial pentru medic în luarea deciziei privind eficacitatea imunoterapiei cu inhibitori PD-1. Pacientele cu un CPS de ≥1 sunt cele mai susceptibile de a beneficia de acest tratament.
Ce șanse de răspuns are imunoterapia și ce înseamnă aceasta pentru supraviețuire?
Studiile clinice majore indică faptul că pacientele cu cancer de col uterin avansat, PD-L1 pozitiv, care primesc imunoterapie combinată cu chimioterapie, prezintă o rată de răspuns superioară (reducerea sau eliminarea tumorilor) și o creștere semnificativă a supraviețuirii în comparație cu terapiile standard. Cu toate acestea, răspunsul este variabil și nu toate pacientele beneficiază, impunând monitorizare riguroasă și reevaluări regulate pentru a ajusta tratamentul.
Cum influențează imunoterapia calitatea vieții?
Comparativ cu chimioterapia, imunoterapia poate avea un impact mai redus asupra calității vieții, deoarece nu determină efecte toxice clasice precum căderea părului, greața severă sau afectarea măduvei osoase. În plus, îmbunătățirea controlului bolii duce la reducerea simptomelor legate de tumori. Totuși, toxicitățile imune și anxietatea legată de un tratament nou pot influența starea generală, motiv pentru care suportul psihologic și comunicarea deschisă cu echipa medicală sunt foarte importante.
Ce se întâmplă dacă boala progresează în ciuda imunoterapiei?
În cazurile în care boala progresează sau reapare după imunoterapie, există multiple opțiuni terapeutice suplimentare, în funcție de starea pacientei și de istoricul tratamentului. Acestea pot include alte regimuri chimioterapice, terapii țintite, participarea la studii clinice cu noi imunoterapice sau terapii combinate, precum și tratamente paliative pentru ameliorarea simptomelor. Este important ca pacientele să rămână în contact constant cu echipa oncologică pentru a beneficia de cele mai noi opțiuni disponibile.
Cum pot accesa imunoterapia pacientele oncologice din România?
Accesul la imunoterapie în România se extinde, fiind inclusă în ghidurile naționale pentru cancerul de col uterin avansat cu PD-L1 pozitiv. Pacientele trebuie evaluate în centre oncologice de referință pentru testarea biomarkerilor și inițierea tratamentului. Participarea în studii clinice este o altă opțiune importantă. Pacientele sunt sfătuite să ceară informații de la medici și asociații.
Ce recomandări există privind monitorizarea și urmărirea pacientelor sub imunoterapie?
Monitorizarea imunoterapiei este riguroasă și multidisciplinară, implicând evaluări clinice, imagistice și de laborator (pentru toxicități). Screening-ul funcțiilor hepatice, renale, tiroidiene și semnele inflamatorii sunt esențiale, alături de comunicarea deschisă cu pacienta, pentru gestionarea eficientă a terapiei.
Ce poate face pacienta informată?
Pacienta cu cancer de col uterin persistent/recurent/metastatic trebuie să întrebe despre imunoterapia cu pembrolizumab, să solicite testarea PD-L1 și biomarkeri, să discute riscurile/beneficiile multidisciplinar, să monitorizeze reacțiile adverse imune și să întrebe despre studiile clinice, continuând evaluările periodice.
REFERINȚE
1. Cancer Research UK
https://www.cancerresearchuk.org/about-cancer/cervical-cancer/treatment/targeted-immunotherapy-drugs
2. Cancer Council https://www.cancercouncil.com.au/cervical-cancer/treatment/immunotherapy/
3. Dey T, Agrawal S. Immunotherapy in cervical cancer: an innovative approach for better treatment outcomes. Explor Target Antitumor Ther. 2025 Mar 2;6:1002296. doi: 10.37349/etat.2025.1002296. PMID: 40061136; PMCID: PMC11886377.
4. Tewari, Krishnansu S et al. Immunotherapy plus chemoradiotherapy in cervical cancer management
The Lancet, Volume 403, Issue 10434, 1310 – 1311
5. Grau-Bejar JF, Garcia-Duran C, Garcia-Illescas D, Mirallas O, Oaknin A. Advances in immunotherapy for cervical cancer. Ther Adv Med Oncol. 2023 Mar 28;15:17588359231163836. doi: 10.1177/17588359231163836. PMID: 37007635; PMCID: PMC10052578.
6. Zhao Z, Ruan J, Fang M, Liu J, Liao G. Efficacy and safety of chemoradiotherapy plus immune checkpoint inhibitors for the treatment of locally advanced cervical cancer: a systematic review and meta-analysis. Front Immunol. 2024 Sep 16;15:1459693. doi: 10.3389/fimmu.2024.1459693. Erratum in: Front Immunol. 2024 Nov 20;15:1524791. doi: 10.3389/fimmu.2024.1524791. PMID: 39351236; PMCID: PMC11439685.
7. Kim YM, Nishio S, Kim SI, Hasegawa K, Dubot C, Cáceres MV, Tewari KS, Lorusso D, Lee JW, Liou WS, Li K, Tekin C, Colombo N, Monk BJ. Pembrolizumab plus chemotherapy with or without bevacizumab in East Asian participants with persistent, recurrent, or metastatic cervical cancer: results from KEYNOTE-826 final analysis. J Gynecol Oncol. 2025 Jul;36(4):e110. doi: 10.3802/jgo.2025.36.e110. PMID: 40590325; PMCID: PMC12226315.
8. Naumann RW, Hollebecque A, Meyer T, Devlin MJ, Oaknin A, Kerger J, López-Picazo JM, Machiels JP, Delord JP, Evans TRJ, Boni V, Calvo E, Topalian SL, Chen T, Soumaoro I, Li B, Gu J, Zwirtes R, Moore KN. Safety and Efficacy of Nivolumab Monotherapy in Recurrent or Metastatic Cervical, Vaginal, or Vulvar Carcinoma: Results From the Phase I/II CheckMate 358 Trial. J Clin Oncol. 2019 Nov 1;37(31):2825-2834. doi: 10.1200/JCO.19.00739. Epub 2019 Sep 5. PMID: 31487218; PMCID: PMC6823884.
9. Rodrigues M, Vanoni G, Loap P, Dubot C, Timperi E, Minsat M, Bazire L, Durdux C, Fourchotte V, Laas E, Pouget N, Castel-Ajgal Z, Marret G, Lesage L, Meseure D, Vincent-Salomon A, Lecompte L, Servant N, Vacher S, Bieche I, Malhaire C, Huchet V, Champion L, Kamal M, Amigorena S, Lantz O, Chevrier M, Romano E. Nivolumab plus chemoradiotherapy in locally-advanced cervical cancer: the NICOL phase 1 trial. Nat Commun. 2023 Jun 22;14(1):3698. doi: 10.1038/s41467-023-39383-8. PMID: 37349318; PMCID: PMC10287640.
10. Lee SJ, Yoo JG, Kim JH, Park JY, Lee JY, Lee YY, Suh DH. Gynecologic oncology in 2024: breakthrough trials and evolving treatment strategies for cervical, uterine corpus, and ovarian cancers. J Gynecol Oncol. 2025 Jan;36(1):e72. doi: 10.3802/jgo.2025.36.e72. PMID: 39900347; PMCID: PMC11790998.
